2025ASCO开幕!恒瑞医药15款抗肿瘤创新药70项研究成果亮相
芝加哥当地时间5月31日,2025年美国临床肿瘤学会(ASCO年会正式开幕。作为**肿瘤学领域最权威、**影响力的年度盛会之一,全球**专家齐聚于此,探讨、分享当前**最前沿的肿瘤学科研成果和肿瘤**技术。
恒瑞医药已连续15年携重磅研究成果参加ASCO年会。本届年会,恒瑞医药共有72项研究入选,其中创新药研究70项。包括4项口头报告(Oral、5项快速口头报告(Rapid Oral、27项壁报展示(Poster、36项线上发表(Publication Only[1]。研究成果涵盖消化系统肿瘤、乳腺癌、肺癌、妇科肿瘤、泌尿肿瘤、黑色素瘤、头颈肿瘤、肉瘤、鼻咽癌、血液肿瘤和硬纤维瘤等十余个肿瘤**领域。
涉及的创新药包括8款已上市创新产品:注射用卡瑞利珠单抗(艾瑞卡®)、甲磺酸阿帕替尼片(艾坦®)、马来酸吡咯替尼片(艾瑞妮®)、羟乙磺酸达尔西利片(艾瑞康®)、阿得贝利单抗注射液(艾瑞利®)、氟唑帕利胶囊(艾瑞颐®)、注射用瑞康曲妥珠单抗(艾维达®,研发代号:SHR-A1811、苹果酸法米替尼胶囊(艾比特®),以及7款未上市创新产品:抗PD-L1/**F-βRII双抗瑞拉芙普-α(SHR-1701、IL-15融合蛋白SHR-1501、双特异性抗体SHR-2017、全人源抗CTLA-4单克隆抗体SHR-8068、抗体偶联**(ADCSHR-1826、SHR-A1912、SHR-A2102。2类新药盐酸伊立替康脂质体注射液(II(越优力®)及**首仿药昂丹司琼口溶膜(艾其速®)各有1项研究入选。
01
9项研究入选口头报告和快速口头报告
凸显恒瑞硬核研发实力
本次ASCO年会,恒瑞医药4项研究入选口头报告,5项研究入选快速口头报告,创新药成果涵盖多个前沿**领域,其学术价值与临床意义获得**同行高度认可,不仅体现了公司在抗肿瘤新药研发领域的****水平,更向全球学术界展示了**医药创新的硬核实力。
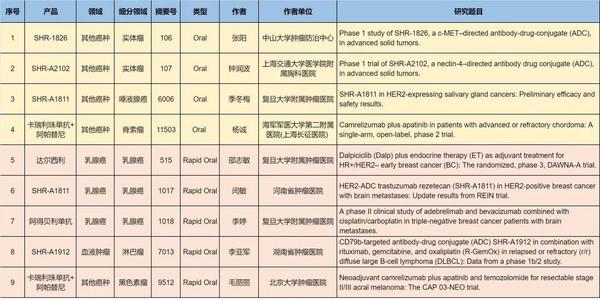
由中山大学肿瘤防治**徐瑞华教授牵头,恒瑞自主研发的靶向c-MET ADC**SHR-1826**实体瘤的一项I期临床研究成功入选口头报告[2]。该研究共纳入116例受试者,其中非小细胞肺癌(NSCLC受试者72例。44%的受试者既往接受过≥3线的系统性抗肿瘤**。在58例可评估的NSCLC患者中,客观缓解率(ORR达39.7%,疾病控制率(DCR达94.8%。疗效覆盖不同c-MET表达水平患者。在所有的72例NSCLC中,中位无进展生存期(PFS为6.8个月(95% CI,4.5–7.2。该研究结果表明,SHR-1826在重度经治的实体瘤患者中展现出良好的安全性和耐受性;在NSCLC患者中表现出富有前景的抗肿瘤活性和**缓解的潜力,且疗效不严格依赖于MET的高表达水平,有望进一步研究给广大患者带来新的福音。
由上海交通大学附属胸科医院钟华教授、钟润波教授团队开展的一项Nectin-4靶向抗体偶联**SHR-A2102**晚期实体瘤患者的I期研究成功入选口头报告[3]。该研究共纳入369例晚期实体瘤患者,中位年龄59岁;ECOG PS 1分85.6%;64.0%的患者接受过≥2线既往系统性**。在304例可评估疗效的患者中,ORR为35.2%(95% CI,29.8-40.9,DCR为84.2%(95% CI,79.6-88.1。SHR-A2102在多种肿瘤类型中均表现出具有临床意义的抗肿瘤活性,不同亚型NSCLC的ORR为25%-43.5%;三阴性乳腺癌(TNBC与HR阳性/HER2阴性乳腺癌ORR分别达56%与65%;头颈部鳞状细胞癌(HNSCCORR达50%。所有瘤种的DCR为73%-100%,显示出广泛的疾病控制能力。该研究结果表明,SHR-A2102在经多线**的实体瘤患者中展现出可控的安全性和广谱抗肿瘤活性。
由复旦大学附属肿瘤医院季冬梅教授团队开展的一项瑞康曲妥珠单抗(SHR-A1811**唾液腺癌的研究成功入选口头报告[4]。该研究共纳入33例晚期唾液腺癌患者,其中21例HER2过表达患者ORR为85.7%,DCR为100%;12例HER2低表达患者ORR为30.0%,DCR为100%。没有患者因**相关不良事件(TRAE而停止**。该研究结果表明,SHR-A1811在HER2阳性和HER2低表达的晚期唾液腺癌中显示出有希望的疗效,并具有可控的安全性。
由海军军医大学第二附属医院(上海长征医院肖建如教授、杨诚教授团队开展的卡瑞利珠单抗联合阿帕替尼**晚期或难治性脊索瘤的单臂、开放标签、Ⅱ期研究成功入选口头报告[5]。该研究共有33例患者纳入疗效与安全性分析。根据RECIST 1.1,7例患者(21.2%,[95% CI,9.0-38.9]达到部分缓解(PR,6个月DCR为85.2%(23/27,中位PFS为18.1个月(95% CI,11.0-28.5。根据Choi标准,16例患者(48.5%,[95% CI,30.8-66.5]达到PR,6个月DCR为77.7%(21/27,中位PFS为15.3个月(95% CI,10.6-NE。研究结果表明,卡瑞利珠单抗联合阿帕替尼在脊索瘤的**中展现出良好的疗效与可控的安全性。
02
乳腺癌领域:
吡咯替尼、达尔西利****新突破
在乳腺癌领域,吡咯替尼、达尔西利、卡瑞利珠单抗、阿帕替尼、阿得贝利单抗、瑞康曲妥珠单抗(SHR-A1811、SHR-2017,或产品间联合或联合化疗,共有19项研究入选(包括3项快速口头报道和7项壁报展示以及9项线上发表。其中吡咯替尼占据7项、达尔西利占据6项,进一步巩固其在乳腺癌**中的地位。此外,瑞康曲妥珠单抗(SHR-A1811、阿得贝利单抗相关研究入选快速口头报告,获得业内广泛关注。
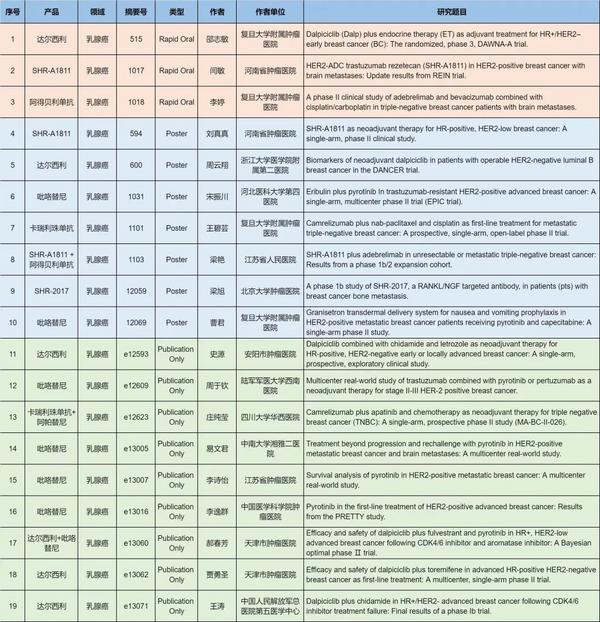
由复旦大学附属肿瘤医院邵志敏教授团队、天津市肿瘤医院郝继辉教授团队开展的DAWNA-A研究:达尔西利(Dalp联合内分泌**(ET用于HR /HER2-早期乳腺癌的III期随机对照研究的**中期分析结果成功入选快速口头报告[6]。该研究共纳入5274例患者,Dalp ET组的侵袭性无病生存期(iDFS显著优于安慰剂 ET组HR=0.56(95% CI,0.43–0.71,iDFS获益在各分层因素及基线亚组中表现一致;次要终点无病生存期(DFS和远处无病生存期(DDFS均支持Dalp ET组的疗效优势。该研究结果表明,在ET**的基础上增加联合达尔西利能显著改善iDFS,且安全性可耐受。
由河南省肿瘤医院闫敏教授团队牵头开展的瑞康曲妥珠单抗(SHR-A1811**HER2阳性乳腺癌脑转移的**结果成功入选快速口头报告[7]。该研究评估了SHR-A1811单药或联合贝伐珠单抗**HER2阳性乳腺癌脑转移(BCBM的疗效与安全性。共入组58例患者,96.6%曾接受抗HER2**。截至2024年12月31日,确认的颅内ORR:单药组为84.4%,联合**组为72.7%;两组DCR均为100%;单药组中位PFS为13.2个月,联合**组尚未成熟。该研究结果表明,SHR-A1811单药或联合贝伐珠单抗均可获得较高的颅内缓解率。
由复旦大学附属肿瘤医院张剑教授团队牵头开展的阿得贝利单抗联合贝伐珠单抗及顺铂/卡铂**合并脑转移的三阴性乳腺癌(TNBC患者的II期临床研究成功入选快速口头报告[8]。研究共入组35例伴有活动性脑转移的TNBC患者,所有患者接受阿得贝利单抗、贝伐珠单抗,以及顺铂或卡铂的三联**方案。在ITT人群中,**神经系统客观缓解率(CNS-ORR为77.1%,经确认的CNS-ORR为71.4%。在23例发生疾病进展的患者中,69.6%的患者**进展发生在脑部。中位PFS为7.6个月(95% CI,5.7-11.5,而CNS-PFS为10个月(95% CI,7.4-12.6,中位OS为16个月(95% CI,11.7至未达到。研究结果表明,阿得贝利单抗联合贝伐珠单抗及顺铂/卡铂展现出良好的颅内抗肿瘤活性,能够延长**神经系统无进展生存期(CNS-PFS和OS,且具有良好的安全性。
03
消化系统肿瘤领域:
卡瑞利珠单抗续写新篇章
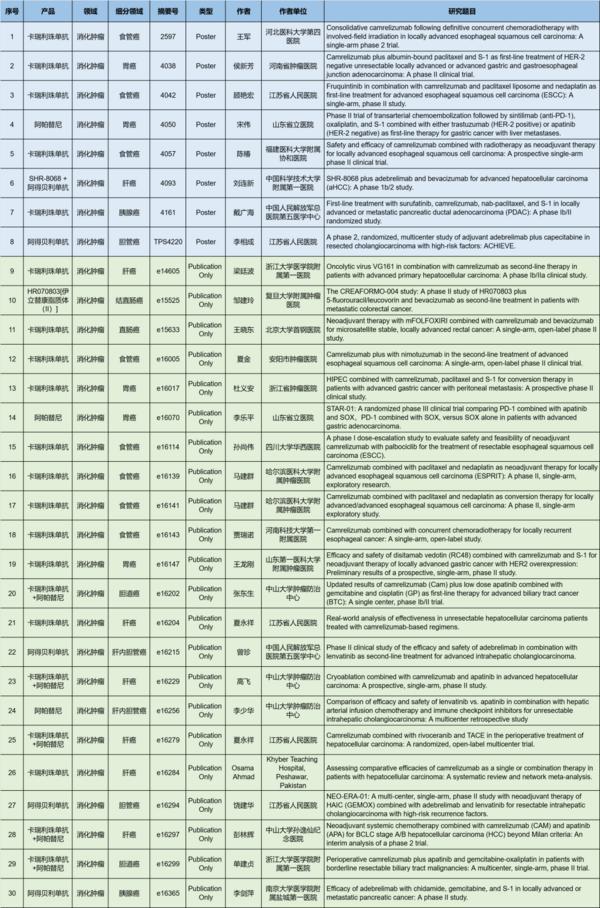
在消化系统肿瘤领域,卡瑞利珠单抗、阿帕替尼、阿得贝利单抗、SHR-8068等**,共有30项研究入选(包括8项壁报和22项线上发表。其中卡瑞利珠单抗占据21项,**展现其显著特点与潜力,再次成为ASCO舞台焦点之一,续写国产PD-1抑制剂新篇章。此外,近年来在肺癌领域取得一系列突破的阿得贝利单抗也在积极探索新的适应症,本次ASCO大会分别有**、胆管癌、胰腺癌等5项相关研究入选。这些新老**前沿研究的不断出现,有望为消化系统肿瘤患者带来更多获益!
04
其他肿瘤领域:
多点开花,彰显**竞争力
在肺癌、妇科肿瘤、淋巴瘤、**癌、头颈肿瘤、黑色素瘤、肉瘤、鼻咽癌、脊索瘤、唾液腺癌、胸腺癌、硬纤维瘤、涎腺导管癌等其他多个疾病领域,卡瑞利珠单抗、阿帕替尼、阿得贝利单抗、吡咯替尼、达尔西利、氟唑帕利、法米替尼、瑞康曲妥珠单抗(SHR-A1811、SHR-1501、瑞拉芙普-α(SHR-1701、SHR-1826、SHR-A1912、SHR-A2102等抗肿瘤创新药相关研究一共入选了4项口头报告、2项快速口头报告、12项壁报展示和4项线上发表,彰显了恒瑞医药强劲的研发实力。此外,昂丹司琼口溶膜在防治化疗导致的恶心呕吐方面展现出了良好的疗效,本次ASCO年会有1项研究线上发表。
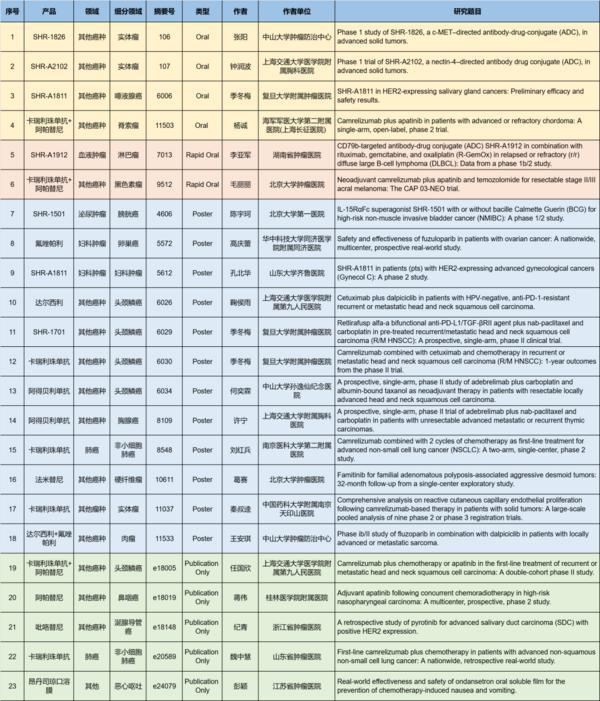
由北京大学肿瘤医院宋玉琴教授团队牵头开展的“SHR-A1912联合**在B细胞非霍奇金淋巴瘤中的Ib/II期研究”入选大会快速口头报告[9]。剂量递增阶段的结果显示,1.8 mg/kg为SHR-A1912与R-GemOx联合**B细胞非霍奇金淋巴瘤的Ⅱ期试验推荐剂量(RP2D。共有37例复发难治弥漫大B细胞淋巴瘤(DLBCL患者接受了SHR-A1912 1.8 mg/kg联合R-GemOx方案(利妥昔单抗、吉西他滨、奥沙利铂**(62.2%的受试者对上一线**难治,56.8%的受试者为原发难治,ORR为70.3%(95% CI,53.0-84.1,**缓解率(CRR为54.1%(95% CI,36.9-70.5,6个月持续缓解率为95.5%(95% CI,71.9-99.3。研究结果表明,SHR-A1912联合R-GemOx展现出强大的抗肿瘤活性,有望成为复发难治DLBCL患者的新的**选择,进一步改善患者的预后。
由北京大学肿瘤医院郭军教授团队开展的“卡瑞利珠单抗联合阿帕替尼、替莫唑胺新辅助**可切除的Ⅱ/Ⅲ期肢端黑色素瘤:CAP 03-NEO研究”成功入选大会快速口头报告[10]。在研究**阶段接受手术的28例患者中,16例(57.1%出现病理缓解,其中7例(25.0%病理**缓解(pCR,5例接近pCR,4例病理部分缓解(pPR。此外,12例患者(42.9%实现了主要病理缓解(MPR。截止到2025年4月,中位无事件生存期(EFS尚未到达,12个月的EFS率为77.6%(95% CI,56.7- 89.3%。新辅助**并未增加手术并发症。该研究结果表明,卡瑞利珠单抗联合阿帕替尼、替莫唑胺新辅助**可切除的Ⅱ/Ⅲ期肢端黑色素瘤具有前景,支持该研究进入第二阶段以进一步评估其**Ⅲ期患者的疗效与安全性。
《“健康**2030”规划纲要》提出到2030年,要实现总体癌症5年生存率提高15%的战略目标。抗肿瘤**是癌症患者控制和**疾病的重要希望。作为创新型**化制药企业,恒瑞医药长期坚持“科技为本,为人类创造健康生活”的使命,针对肿瘤等严重威胁人类生命健康的疾病开展科研攻关,已上市的23款创新药中抗肿瘤创新药占比过半。公司另有90多个自主创新产品正在临床开发,近400多项临床试验在**外开展。
恒瑞医药连续15年携创新产品研究成果登上ASCO年会,体现了公司强大的抗肿瘤**研发实力,也让**肿瘤学界看到更多**力量。未来,恒瑞医药将继续坚持“以患者为**”的理念,力争研制出更多的新药、好药,服务“健康**”,惠及全球患者。

